
脳卒中を発症すると、感覚障害(かんかくしょうがい)が表れることがあります。
感覚障害とは、『触られている感覚がない』など、身体に感じるはずの刺激を正確に認識できなくなる症状です。
この感覚の変化により、
- ⚫︎ 歩いているときに麻痺した足に体重がかかっているかどうか分からない
- ⚫︎ 脚を動かしている感覚がない
- ⚫︎ 足が物にぶつかって怪我をしても気づかない
といった問題が生じることがあります。
さらに、感覚障害は上肢の運動機能とも密接に関係していることが明らかになっています。
Meyer S(2014)は、感覚の鋭敏さが上肢の機能回復に影響を与えるのかどうかを調べた結果、興味深い報告をしています。
例えば、
- ⚫︎ 二点識別覚が良好な患者は、脳卒中後3ヶ月や6ヶ月で上肢の器用さを獲得する可能性が高い
- ⚫︎ 感覚を司る脳領域の活動が残っている患者は、6ヶ月や12ヶ月後により良好な上肢の運動機能を示す
- ⚫︎ 深部感覚が保たれている患者は、上肢の動きの質が高い
などです。
また、感覚障害は歩行能力とも関連があるとされています。
Tyson SF(2008)の研究では、感覚障害が強い人は移動能力が低下する傾向があることが報告されており、歩行障害との関連も示唆されています。
このように、感覚障害は単に『触られた感じが分からない』だけにとどまらず、上肢の運動や歩行にも影響を及ぼしている可能性があります。
そのため、手や歩行を改善するために感覚障害の影響を評価し、対応することは重要です。
しかし、感覚障害に特化したリハビリを受ける機会が少ないと感じたことはありませんか?
その背景には、感覚障害のリハビリに関するエビデンスの不足や、確立された方法がまだ存在しないという課題があります。
とはいえ、まったく情報がないわけではありません。
実は、海外の研究では感覚障害のリハビリがいくつか報告されています。
今回は、それらの情報をもとに、脳卒中後の感覚障害を改善させるためのリハビリを6つ紹介します。
情報の信頼性について
・本記事はBRAIN代表/理学療法士の針谷が執筆しています(執筆者情報は記事最下部)。
・本記事の情報は、基本的に信頼性の高いシステマティックレビュー研究、臨床研究から得られたデータを引用しています。
リハビリの無料体験を実施中!
といった方から選ばれています!

BRAINアカデミー
エビデンスに基づく脳卒中リハビリテーションを体系的・網羅的に学ぶ、3ヶ月間のオンライン学習プログラムです。①動画教材 ②課題 ③フィードバックを通じて、EBMを身に付けましょう!
詳細はこちら

書籍|文献検索の超基本
「先輩に聞けばいい」から卒業しませんか?
本書は、PT・OT・STが最短で文献検索を身につけるための一冊です。172ページ+40本の動画で、PubMed検索からAI活用まで実践的に学べます。ChatGPT、Elicit、Semantic ScholarなどのAIツールを“なんとなく使う”のではなく、正しく臨床に活かす方法を体系的に解説。文献検索は、早く身につけた人が圧倒的に伸びます。エビデンスを自分で調べられるセラピストになりませんか?
脳卒中後の感覚障害に対するリハビリ7選
感覚障害に有効なリハビリは以下の通りです。
- ⚫︎ TMS(上肢)
- ⚫︎ 摩擦刺激(上肢)
- ⚫︎ 感覚識別課題(上肢)
- ⚫︎ 電気刺激(上肢・下肢)
- ⚫︎ 他動反復運動(下肢)
- ⚫︎ 運動イメージ+感覚トレーニング(下肢)
- ⚫︎ 閉眼トレッドミルトレーニング(下肢)
詳しく解説します。
脳卒中後の麻痺側上肢の感覚障害に有効なリハビリ

TMS

Chen G(2022)は、世界中の文献をまとめるシステマティックレビュー研究を通して、TMSが脳卒中後の感覚障害を改善させる上で有効であることを報告しました。
なお、10回未満の刺激では有効とは言えないという結果になっており注意が必要です。
また、高頻度TMS(HF-TMS)が麻痺側上肢の感覚障害を改善させる上で有効であることが報告されています。
Pundik S(2021)は、発症から平均45ヶ月経過した慢性期脳卒中患者16人を対象にし、高頻度TMS(HF-TMS) +電気刺激+振動刺激を組み合わせることの有効性を検証しました。
HF-TMSは、一次体性感覚皮質(S1)をターゲットにし、麻痺側の手に感覚レベルの電気刺激と振動刺激を同時に行いながら実施されました。
結果として、麻痺側の感覚障害(二点識別覚)の改善において有効であることを報告しました。
なお、TMSには高頻度TMSの他、低頻度TMSやシータバースト刺激といったいくつかの刺激タイプがあります。
刺激タイプを間違えると有効とは言えなくなりますのでご注意ください。
▶︎TMSについて詳しく知りたい方はこちらの動画をご覧ください
摩擦刺激
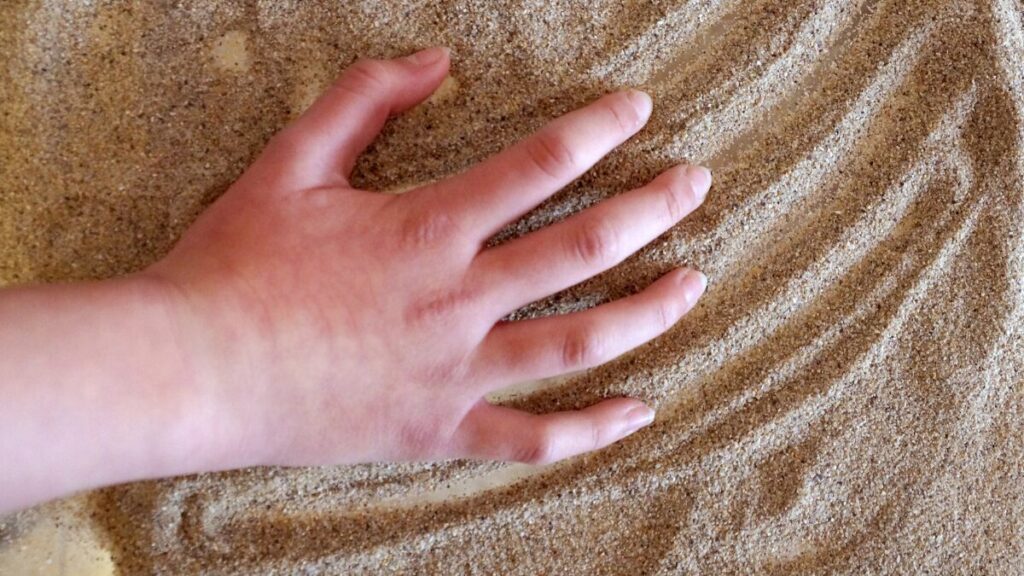
Vidovič M(2025)は、慢性期の脳卒中患者36人を対象に、砂で皮膚を摩擦する『摩擦刺激』の効果を調査しました。
この研究では対象者36人を3つのグループに分け、その中の1つのグループにだけ、摩擦刺激を1回15分追加しています。
結果として、摩擦刺激を行った1つのグループだけに感覚障害の改善が認められました。
このことから、摩擦刺激は感覚障害を改善させる上で有効な手段と考えられています。
感覚識別課題

感覚識別課題というのは、身体に触れている物体が何か、あるいは物体の硬さや大きさ、材質や形状などについて識別する課題です。
Carey L(2011)は、発症から平均48.14ヶ月経過した慢性期脳卒中患者50人を対象にし、 「SENSe」というリハビリプログラムの効果を検証しました。
このプログラムでは、主に次の3つの感覚をトレーニングします。
- ⚫︎ 質感の識別:目を閉じて、布や木など、異なる素材を触って区別する訓練をします。
- ⚫︎ 身体の位置の感覚:目を閉じて、腕や足を動かしてもらい、どの位置にあるかを当てる訓練をします。
- ⚫︎ 触覚で物体を認識する:目を閉じて、色々な形の物体を触って、それが何であるかを当てる訓練をします。
また、トレーニング中は以下の点に注意します。
- ⚫︎ 難易度調整:最初は簡単な課題から始め、徐々に難易度を上げる
- ⚫︎ 閉眼:目を閉じて行うことで、触覚に集中しやすくする
- ⚫︎ フィードバック:間違えた時は、正しい答えを教えてもらったり、見本を見せてもらったりして、感覚を修正する
- ⚫︎ 反復:繰り返し練習することで、脳に感覚を学習させていきます。
結果として、SENseは感覚障害を改善させる上で有効であることを報告しました。
電気刺激
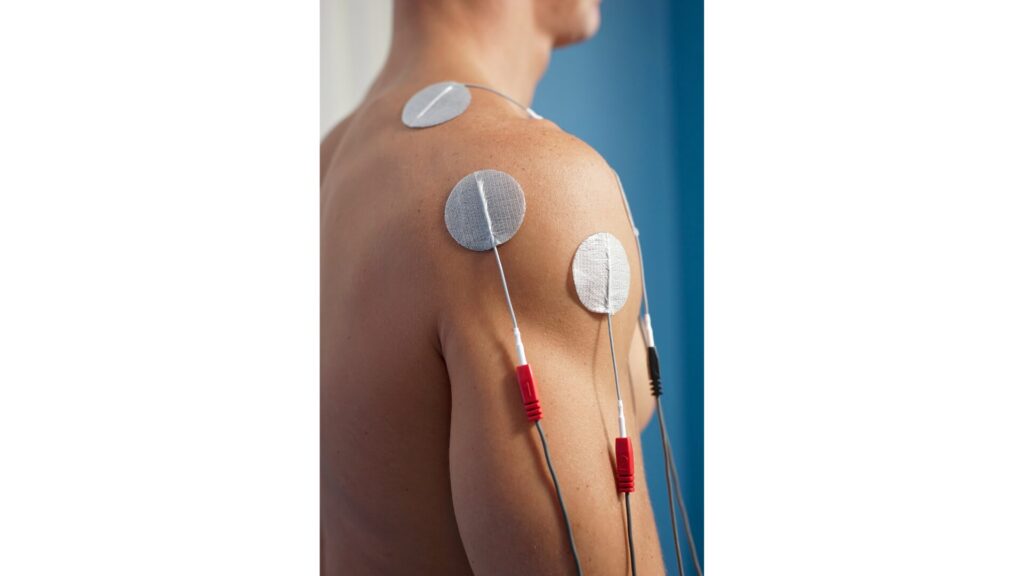
Peurala SH(2002)は、発症から平均3.3年経過した慢性期脳卒中患者59人を対象にし、電気刺激の効果を検証しました。
電気刺激は、特殊な手袋電極を介して、1日2回、20分間ずつ実施されました。
結果として、電気刺激は上肢の表在感覚の改善に有効であることが報告されました。
脳卒中後の麻痺側下肢の感覚障害に有効なリハビリ

電気刺激
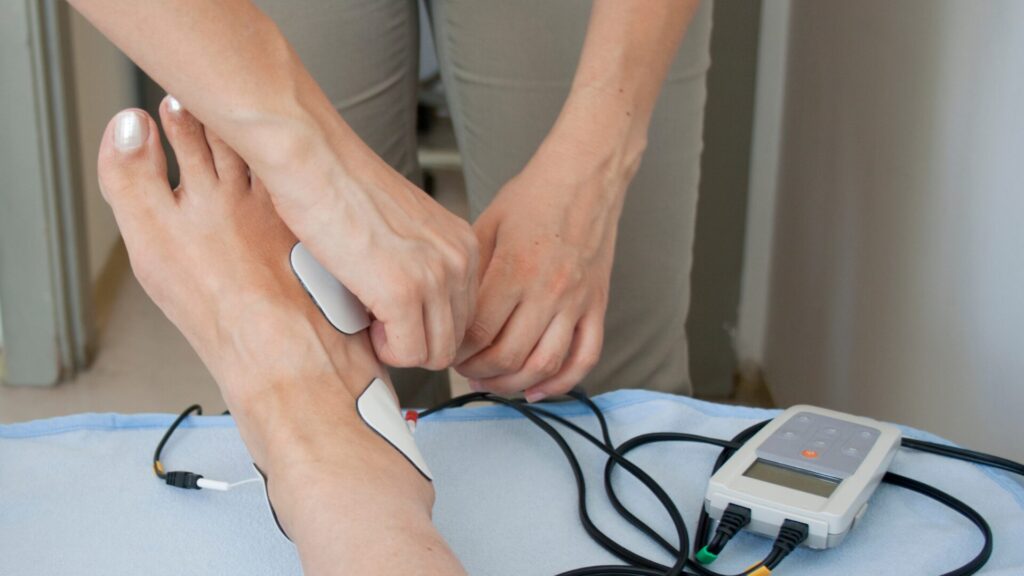
さきほど紹介したPeurala SH(2002)の研究では、下肢の感覚障害も改善させたことを報告しています。
Peurala SH(2002)は、発症から平均3.3年経過した慢性期脳卒中患者59人を対象にし、電気刺激の効果を検証しました。
電気刺激は、特殊な靴下電極を介して、1日2回、20分間ずつ実施されました。
結果として、電気刺激は表在感覚の改善に有効であることが報告されました。
なお、その他にも運動機能や痙縮、歩行速度の向上を認めました。
Tyson SF(2013)は、脳卒中患者29人を対象にし、電気刺激の効果を検証しました。
電気刺激は、TENSという電気刺激を、特殊な靴下電極を介して約2時間にわたり実施しました。
結果として、電気刺激は足関節の深部感覚の向上において有効であることを報告しました。
反復他動運動

Kwon OS(2013)は、発症から平均10.43ヶ月経過した脳卒中患者45人を対象にし、反復的な他動運動と自動運動)の効果を検証しました。
他動運動と自動運動とは?
自分で動かさない運動を他動運動、自分で動かす運動を自動運動と言います。”自分で動かさない運動”というのは、他の人に動かされる、あるいはロボットなどの機器によって動かされるものを指します。
反復的な他動運動は、バイオデックスという機器を用いて、膝関節の屈伸運動を10度から100度の範囲で、角度速度120度/秒で60回反復して行われました。
結果として、反復的な他動運動は、膝関節の深部感覚(位置覚)を改善させる上で有効であることを報告しました。
運動イメージ+感覚トレーニング

Lee H(2015)は、脳卒中患者36人を対象にし、運動イメージ+感覚トレーニングの効果を検証しました。
感覚トレーニング(25分)は、バランスパッドやバランスボード上での立位姿勢や膝の屈伸運動、体重移動などの課題を行いました。
また、運動イメージ(5分)は、感覚トレーニングで行なった課題を頭の中でイメージすることで行われました。
結果として、バランスや深部感覚(位置覚)の改善に有効であることを報告しました。
閉眼トレッドミルトレーニング

Moon SJ(2015)は、脳卒中患者30人を対象にし、閉眼でのトレッドミルトレーニングの効果を検証しました。
閉眼でのトレッドミルトレーニングは、アイマスクを着用して視覚情報を遮断した状態で、トレッドミル上を歩行練習を行うというものです。
結果として、閉眼トレッドミルトレーニングは膝関節の深部感覚(位置覚)の改善に有効であることを報告しました。
その他
その他、再現性に難しさがあるものの、ロボット+振動刺激(Cordo P, 2009)、水治療法(Han SK, 2013)、などが感覚障害を改善させる上で有効であると報告されています。
視覚や聴覚を活用するのが有効?
また、近年では視覚や聴覚、体性感覚を組み合わせる多感覚統合というアプローチが感覚障害の改善に有効であることが示唆されています(Tinga AM, 2016)。
少し難しい話になりますが、視覚を司る『視覚野』、聴覚を司る『聴覚野』、体性感覚を司る『一次体性感覚野』はつながっていることがわかっています(脳のコネクティビティと言います)。

このつながりは、お互いの活動をサポートすることが知られています。
つまり、脳卒中によって一次体性感覚野の機能が低下し感覚障害が生じても、視覚野や聴覚野からのサポートを受けることによって感覚を感じやすくなる可能性があるということです。
まだ研究段階の分野であり、多感覚統合を活用した確立されたリハビリ方法はありませんが、感覚のリハビリをするときは視覚と聴覚を活用することも検討するとよいでしょう。
感覚刺激を使ったリハビリによる感覚障害以外への効果
運動機能や痙縮の改善
Derakhshanfar M(2020)は、発症から平均20.68ヶ月経過した脳卒中患者30人を対象にし、感覚トレーニングの効果を検証しました。
感覚トレーニングは、6週間、週4日、45分間のセッションで、荷重、ストレッチ圧迫、ブラッシング、アイシングなどを活用して行われました。
結果として、感覚トレーニングは上肢の運動機能や痙縮などにおいて有効であることを報告しました。
バランスの改善
Huzmeli(2017)は、発症から平均40.2ヶ月経過した慢性期脳卒中患者26人を対象にし、大腿部後面に対する感覚トレーニングの効果を検証しました。
なぜ大腿部後面に対して行われたかというと、大腿部後面は、座っているときに椅子やベッドと接している部分であり、大腿部後面の感覚が改善することによって座位バランスにプラスの影響をもたらすと考えられたためです。
感覚トレーニングは、大腿部後面への触覚、振動、圧迫などの刺激、および電気刺激を使って実施されました。
結果として、感覚トレーニングは座位バランスや日常生活動作の自立度を向上させる上で有効であることを報告しました。
Morioka S(2003)は、脳卒中患者26人を対象にし、足底への感覚トレーニングの効果を検証しました。
感覚トレーニングは、厚さ5mm、10mm、15mmの3種類の硬さの異なるスポンジゴムを足の裏に置き、目隠しをした状態で硬さを識別する課題を10日間行いました。
結果として、感覚トレーニングはバランスの向上(立位姿勢における重心動揺/ふらつきの減少)において有効であることを報告しました。
これらの報告を踏まえると、『感覚リハビリによって感覚は改善しなくても運動機能や痙縮、バランスなど他の症状が改善する可能性がある』と言えます。
まとめ
脳卒中後の感覚障害に対するリハビリは、全体的なエビデンスの数が少ないのが現状です。
感覚トレーニングが本当に感覚障害に有効なのかどうかについては意見が分かれており、『感覚トレーニングをすれば感覚障害が改善する』とは言えません(Yilmazer C, 2019; Turville ML, 2019)。
患者さんひとりひとりに合わせて、どの感覚トレーニングを行うのがベストか考える必要があります。
担当セラピストさんと相談しながら、感覚障害の改善に取り組んでみてください。
リハビリの無料体験を実施中!
といった方から選ばれています!

BRAINアカデミー
エビデンスに基づく脳卒中リハビリテーションを体系的・網羅的に学ぶ、3ヶ月間のオンライン学習プログラムです。①動画教材 ②課題 ③フィードバックを通じて、EBMを身に付けましょう!
詳細はこちら

書籍|文献検索の超基本
「先輩に聞けばいい」から卒業しませんか?
本書は、PT・OT・STが最短で文献検索を身につけるための一冊です。172ページ+40本の動画で、PubMed検索からAI活用まで実践的に学べます。ChatGPT、Elicit、Semantic ScholarなどのAIツールを“なんとなく使う”のではなく、正しく臨床に活かす方法を体系的に解説。文献検索は、早く身につけた人が圧倒的に伸びます。エビデンスを自分で調べられるセラピストになりませんか?
参考文献
Meyer S, Karttunen AH, Thijs V, Feys H, Verheyden G. How do somatosensory deficits in the arm and hand relate to upper limb impairment, activity, and participation problems after stroke? A systematic review. Phys Ther. 2014 Sep;94(9):1220-31. doi: 10.2522/ptj.20130271. Epub 2014 Apr 24. PMID: 24764072.
Tyson SF, Hanley M, Chillala J, Selley AB, Tallis RC. Sensory loss in hospital-admitted people with stroke: Characteristics, associated factors, and relationship with function. Neurorehabil Neural Repair. 2008;22(2):166–172. doi:10.1177/1545968307305523.
Chia FS, Kuys S, Low Choy N. Sensory retraining of the leg after stroke: systematic review and meta-analysis. Clin Rehabil. 2019 Jun;33(6):964-979.
Pundik S, Skelly M, McCabe J, Akbari H, Tatsuoka C, Plow EB. Does rTMS Targeting Contralesional S1 Enhance Upper Limb Somatosensory Function in Chronic Stroke? A Proof-of-Principle Study. Neurorehabil Neural Repair. 2021 Mar;35(3):233-246. doi: 10.1177/1545968321989338. Epub 2021 Jan 29. PMID: 33514270; PMCID: PMC7933056.
Vidovič M, Vidmar G, Kafel T, Šuc L, Bizovičar N. The effects of tactile stimulation and transcutaneous electrical nerve stimulation on upper limb function and daily activities in patients with stroke: a randomized controlled trial. Int J Rehabil Res. 2025 Jun 1;48(2):90-99.
Carey L, Macdonell R, Matyas TA. SENSe: Study of the Effectiveness of Neurorehabilitation on Sensation: a randomized controlled trial. Neurorehabil Neural Repair. 2011 May;25(4):304-13. doi: 10.1177/1545968310397705. Epub 2011 Feb 24. PMID: 21350049.
Peurala SH, Pitkänen K, Sivenius J, Tarkka IM. Cutaneous electrical stimulation may enhance sensorimotor recovery in chronic stroke. Clin Rehabil. 2002 Nov;16(7):709-16. doi: 10.1191/0269215502cr543oa. PMID: 12428819.
Tyson SF, Sadeghi-Demneh E, Nester CJ. The effects of transcutaneous electrical nerve stimulation on strength, proprioception, balance and mobility in people with stroke: a randomized controlled cross-over trial. Clin Rehabil. 2013 Sep;27(9):785-91. doi: 10.1177/0269215513478227. Epub 2013 Mar 15. PMID: 23503739.
Kwon OS, Lee SW. Effect of continuing repeated passive and active exercises on knee’s position senses in patients with hemiplegia. NeuroRehabilitation. 2013;33(3):391-7. doi: 10.3233/NRE-130969. PMID: 23949071.
Lee H, Kim H, Ahn M, You Y. Effects of proprioception training with exercise imagery on balance ability of stroke patients. J Phys Ther Sci. 2015 Jan;27(1):1-4. doi: 10.1589/jpts.27.1. Epub 2015 Jan 9. PMID: 25642023; PMCID: PMC4305533.
Moon SJ, Kim YW. Effect of blocked vision treadmill training on knee joint proprioception of patients with chronic stroke. J Phys Ther Sci. 2015 Mar;27(3):897-900. doi: 10.1589/jpts.27.897. Epub 2015 Mar 31. PMID: 25931754; PMCID: PMC4395738.
Cordo P, Lutsep H, Cordo L, Wright WG, Cacciatore T, Skoss R. Assisted movement with enhanced sensation (AMES): coupling motor and sensory to remediate motor deficits in chronic stroke patients. Neurorehabil Neural Repair. 2009 Jan;23(1):67-77. doi: 10.1177/1545968308317437. Epub 2008 Jul 21. PMID: 18645190.
Han SK, Kim MC, An CS. Comparison of effects of a proprioceptive exercise program in water and on land the balance of chronic stroke patients. J Phys Ther Sci. 2013 Oct;25(10):1219-22. doi: 10.1589/jpts.25.1219. Epub 2013 Nov 20. PMID: 24259761; PMCID: PMC3820184.
Tinga AM, Visser-Meily JM, van der Smagt MJ, Van der Stigchel S, van Ee R, Nijboer TC. Multisensory Stimulation to Improve Low- and Higher-Level Sensory Deficits after Stroke: A Systematic Review. Neuropsychol Rev. 2016 Mar;26(1):73-91.
Derakhshanfar M, Raji P, Bagheri H, Jalili M, Tarhsaz H. Sensory interventions on motor function, activities of daily living, and spasticity of the upper limb in people with stroke: A randomized clinical trial. J Hand Ther. 2021 Oct-Dec;34(4):515-520. doi: 10.1016/j.jht.2020.03.028. Epub 2020 Jun 18. PMID: 32565102.
Dogru Huzmeli E, Yildirim SA, Kilinc M. Effect of sensory training of the posterior thigh on trunk control and upper extremity functions in stroke patients. Neurol Sci. 2017 Apr;38(4):651-657. doi: 10.1007/s10072-017-2822-z. Epub 2017 Jan 30. PMID: 28138865.
Morioka S, Yagi F. Effects of perceptual learning exercises on standing balance using a hardness discrimination task in hemiplegic patients following stroke: a randomized controlled pilot trial. Clin Rehabil. 2003 Sep;17(6):600-7. doi: 10.1191/0269215503cr654oa. PMID: 12971704.
Yilmazer C, Boccuni L, Thijs L, Verheyden G. Effectiveness of somatosensory interventions on somatosensory, motor and functional outcomes in the upper limb post-stroke: A systematic review and meta-analysis. NeuroRehabilitation. 2019;44(4):459-477. doi: 10.3233/NRE-192687. PMID: 31256086.
Turville ML, Cahill LS, Matyas TA, Blennerhassett JM, Carey LM. The effectiveness of somatosensory retraining for improving sensory function in the arm following stroke: a systematic review. Clin Rehabil. 2019 May;33(5):834-846. doi: 10.1177/0269215519829795. Epub 2019 Feb 25. PMID: 30798643.











