
脳梗塞や脳出血(以下、脳卒中といいます)を発症すると、歩行障害(ほこうしょうがい)が表れます。
歩行障害によって『ひとりで歩くことができない』などの問題が発生し、日常生活での移動が困難になります。
しかし、海外の研究では、発症6ヶ月時点での歩行自立者の割合は80-90%に上ることが報告されています。
つまり、ほとんどの方は回復期リハビリ病院を退院する頃にはひとりで歩けるようになっているということです。
この背景には、近年の脳卒中歩行リハビリの進歩により、『有効なリハビリ』と『有効でないリハビリ』が明らかになってきたことがあります。
本記事では、世界的に有効性が実証され、治療ガイドラインで推奨されているリハビリ方法を紹介します。
歩行リハビリを行う上で役立つ情報になると思いますので、よかったらご覧ください。
情報の信頼性について
・本記事はBRAIN代表/理学療法士の針谷が執筆しています(執筆者情報は記事最下部)。
・本記事の情報は、基本的に信頼性の高いシステマティックレビュー研究から得られたデータを引用しています。
リハビリの無料体験を実施中!
といった方から選ばれています!

BRAINアカデミー
エビデンスに基づく脳卒中リハビリテーションを体系的・網羅的に学ぶ、6ヶ月間のオンライン学習プログラムです。①動画教材 ②課題 ③フィードバックを通じて、EBMを身に付けましょう!
詳細はこちら

文献検索CAMP
PubMedを使った文献検索を2日でマスターするセラピスト向けオンライン学習プログラムです。AIを活用し、経験1年目の方でも文献検索を行えるレベルまでスキルアップできます。
詳細はこちら
脳梗塞リハビリにおける “歩行練習” まとめ
最初に本記事の結論です。
- 脳卒中後の歩行における問題として『歩行速度』『歩行距離(歩行持久力)』『歩きかた』『歩行自立度』の4つの問題がある
- これらの問題を解決するためには有効性が実証されたリハビリ方法を、適切な条件で行うことが大事
以下、詳しく説明します。
脳卒中後の歩行における問題

脳卒中を発症すると、基本的に以下の4つの問題が生じます。
- ひとりで歩けなくなる(歩行自立度の低下)
- 歩くスピードが遅くなる(歩行速度の低下)
- 歩ける距離が短くなる(歩行持久力の低下)
- 歩きかたが乱れる(歩容の悪化)
みなさまの歩行におけるお困りごとは、この4つのいずれかに含まれているのではないかと思います。
言い換えると、歩行リハビリの目的は、これらの問題を解決することであると言えます。
世界の脳卒中リハビリ研究は、これら4つの問題点を解決するために進歩してきました。
以下、それぞれの問題について詳しく解説します。
ひとりで歩けなくなる(歩行自立度の低下)
脳卒中を発症すると、運動障害や感覚障害、バランス障害などの影響により、一人で歩くことが難しくなります。
ひとりで歩くことが難しいと移動が困難になり、日常生活に大きな制限をもたらします。
しかし、近年の研究では、発症6ヶ月時点でひとりで歩けるようになっている方は80〜90%であるというデータがあり(Lee KB, 2017)、病院を退院する頃には歩けるようになっていることが多いです。
したがって、ひとりで歩くことが難しいのは急性期〜回復期初期であることがほとんどです。
運動機能やバランスなどの向上とともに、ひとりで歩けるようになっていきます。
ひとりで歩けるかどうかを判断するための基準があります(詳しくはこちらの記事をご覧ください)。
最終的には医師の判断を仰ぐことになりますが、基本的には、これらの条件を満たせればお一人で歩いていただいて問題ないと言えます。
歩くスピードが遅くなる(歩行速度の低下)
脳卒中を発症すると、歩行速度が低下します。
一般的に、健常者の歩行速度は1.3m/s程度であることが報告されています(Gomez Bernal A, 2016; Chui KK, 2010)。
これに対し、脳卒中患者さんの歩行速度は低下することが知られています(Sheffler LR, 2015; Balaban B,2014)。
どれくらい歩行速度が低下するかは脳卒中の重症度により異なり、重度歩行障害を有する患者さんは歩行速度が0.1m/sになることもありますし、軽度歩行障害を有する患者さんは1.0m/s以上で歩けることもあります。
脳卒中患者さんがひとりで外出できるようになるための歩行速度の基準値として、0.61〜0.85m/sがあります(An S, 2015; 田代英之, 2015)。
ご自宅から外出されるとき、ある程度の歩行速度が必要です。
例えば、横断歩道を渡るとき、ある程度のスピードで歩けないと、渡っているときに信号が赤へ変わってしまい、横断歩道上に取り残されてしまうということがあります。
また、ご家族やご友人と外出をされる際、周りの方々と歩調を合わせて歩けないことにより、『みんなに気を使わせて申し訳ない』という想いから、家に閉じこもりがちになってしまうことがあります。
これらの例から分かる通り、脳卒中患者さんの歩行速度を向上させることは重要です。
したがって、脳卒中患者さんの歩行リハビリを行う場合は基本的に
- 歩行速度を評価する
- 歩行速度を上げるリハビリを行う
ことが求められます。
歩ける距離が短くなる(歩行持久力の短縮)
脳卒中を発症すると、歩行持久力が低下し、時間あたりの患者さんの歩行距離は短くなります(Sheffler LR, 2015; Balaban B,2014)。
これによって、
- 旅行に行けなくなる
- 会社に出勤できなくなる
- 近くのコンビニまで行けなくなる
のように、日常生活における移動制限が生じます。
脳卒中患者さんの歩ける距離(歩行持久力)については、6分間歩行試験という検査で評価されるのが一般的です。
ひとりで歩けるレベルの患者さんは、平均すると、6分間で352.6m以上歩けるとされています(Kubo H, 2020)。
また、ひとりで外出できるかどうか判断するための閾値として304〜318mが報告されており(Kubo H, 2020; An S, 2015)、ひとりで歩けるようになるためにはある程度の連続歩行距離が必要であると言えます。
このことから、脳卒中患者さんの歩行リハビリを行う場合は基本的に
- 6分間歩行距離を評価する
- 歩行距離を延ばす(持久力を上げる)リハビリを行う
ことが求められます。
歩きかたが乱れる(歩容の悪化)
脳卒中を発症すると、麻痺側の脚でうまく支えられなくなったり、麻痺側の脚を大きく振り出してしまうなど、歩きかたに変化が起こることが知られています(Sheffler LR, 2015; Balaban B,2014)。
また、近年の研究では、脳卒中患者さんの麻痺した脚・足における『推進力の低下』が指摘されています(Roelker SA, 2019)。
麻痺側の推進力(Paretic propulsion)とは?
簡単に言うと、『床を蹴り出す力』のことです。私たち人間が前方へ歩くために必要な要素なのですが、脳卒中患者さんは麻痺側下肢の推進力が低下していることが報告されています。また、この麻痺側の推進力低下によって、種々の代償動作(ぶん回し歩行など)が生じると考えられています。
こういった歩きかたの変化もあってか、脳卒中患者さんは歩行中のエネルギーコストが高いことが知られており(Kramer S, 2016)、疲れやすいと考えられています。
歩きかたが乱れていたとしても、歩くことができれば日常生活を送ることはできます。
しかし、歩きかたが変化することによって、
- 歩くのが恥ずかしい
- 人や物を蹴ってしまう
- 周りから心配されてしまう
といったお困りごとへつながり、QOL(Quality of life:生活の質)が低下することがあります。
このことから、患者さんのご希望に合わせて
- 歩きかたを評価する
- 歩きかたを整えるリハビリを行う
ことが求められます。
以上、脳卒中後の歩行における4つの問題を紹介させていただきました。
脳卒中患者さんの歩行におけるお困り事のほとんどは、これら4つの問題に集約されます。
したがって、これら4つの問題を解決するリハビリを行うことで、脳卒中患者さんの歩行のお困りごとが解決する可能性が高いです。
歩行練習の効果・メリット

脳卒中後の歩行リハビリは、以下の効果があることが報告されています。
- 歩行速度が向上する
- 歩行持久力が向上する
- 歩きかたがよくなる
- 歩行自立度が上がる
上でお伝えした、脳卒中後の歩行における問題に対して有効です。
しかし、歩行をよくするためには、歩行リハビリの『方法』と『頻度』が大事です。
この2つを間違えてしまうと、『リハビリをやったのによくならない』ということになりかねません。
以下、世界的に有効性が実証された歩行リハビリ方法と頻度を紹介します。
脳卒中後の歩行リハビリの方法
有効性が実証されている歩行リハビリ方法は、以下の通りです。
- トレッドミルトレーニング
- 免荷式トレッドミルトレーニング
- 高強度トレーニング
- 有酸素運動と筋力増強訓練
- ロボットアシストトレーニング
- 電気刺激
- 頻回な歩行練習
いずれも、日本脳卒中学会が出版している脳卒中治療ガイドライン2021にて推奨されている方法です。
ガイドラインで推奨されるリハビリ方法は、世界的に有効性が実証されている方法です。
つまり、基本的にガイドラインで推奨されているリハビリを行うことによって、歩行能力が向上する可能性が高いということです。
トレッドミルトレーニング/免荷式トレッドミルトレーニング

トレッドミルトレーニング/免荷式トレッドミルトレーニングとは?
トレッドミルトレーニングは、トレッドミルマシンの上を歩くリハビリです。
マシン上で速度設定を行うことができるため、一定の速度・負荷で歩くことができるのが特長です。
また、トレッドミルトレーニングに免荷装置を付け加えたものを免荷式トレッドミルトレーニングといいます。
身体を吊り上げることによって、体重を軽くして歩く練習を行うことができます。
以下、トレッドミルトレーニングと免荷式トレッドミルトレーニングを合わせて『トレッドミルトレーニング』と言います。
トレッドミルトレーニングの効果・メリット
トレッドミルトレーニングは以下の効果が報告されています(Mehrholz J, 2017; Bishnoi A, 2022; Srivastava, 2016)。
- 歩行速度を向上させる
- 歩行持久力を向上させる
- 歩きかたをきれいにする
- 歩行自立度を向上させる
- 麻痺側下肢の運動機能を向上させる
このように、トレッドミルトレーニングは歩行の4つの問題すべてに対して有効性が認められており、現代においては外すことができない歩行リハビリと言えます。
古典的なリハビリ方法として平地歩行練習があります。
これは、病院や施設の廊下、リハビリ室などの平地を歩く練習のことです。
Nascimento LRら(2021)は、トレッドミルトレーニングは平地歩行練習よりも優れていることを報告しています。
したがって、病院や施設にトレッドミルマシンがあるなら、廊下やリハビリ室内を歩く練習ではなく、トレッドミルトレーニングを行うのが望ましいと言えます。
トレッドミルトレーニングのデメリット
一方で、トレッドミルトレーニングは、
- 歩行見守り以上
- 週3〜5回以上
実施しないと有効とは言えないとされています(Mehrholz J, 2017)
つまり、
- セラピストの介助がないと歩けない患者さん
- 週1〜2回しかリハビリを行えない場合
は、トレッドミルトレーニングによる効果を期待できなくなります。
高強度トレーニング

高強度トレーニングとは?
高強度トレーニングとは、70%HRmax以上の高い強度で行う有酸素運動のことです。
脳卒中リハビリでは、主にトレッドミルトレーニングでキツい運動を行うことを指します。
70%HRmaxは年齢や安静時心拍数によって異なります。
例えば、安静時心拍数70拍/分の場合、年齢ごとの70%HRmaxは以下の通りです。
- 60歳の場合…133拍/分
- 70歳の場合…126拍/分
- 80歳の場合…119拍/分
患者様おひとりおひとりに合った心拍数になるように調整する必要があります。
心拍数の調整は、トレッドミルトレーニング中の速度設定を通して行います。
例えば、心拍数を上げる必要がある場合は、トレッドミルの速度を上げることによって速く歩かなければならない状況をつくります。
高強度トレーニングの効果・メリット
高強度トレーニングには、以下の効果があります(Luo L, 2019; Mah SM, 2020)。
- 歩行速度を向上させる
- 歩行持久力を向上させる
- 歩きかたをきれいにする
特長は効果が高いことであり、通常のトレッドミルトレーニング(40〜50%HRmax)よりもさらに高い効果があることが報告されています。
したがって、歩行を早く大きく改善させたいのであれば、基本的に高強度トレーニングを行うべきと言えるでしょう。
また、高強度トレーニングには、脳由来神経栄養因子(BDNF)の血中濃度を高める効果があることも知られています(Boyne P, 1985; Li X, 2022)。
脳由来神経栄養因子(Brain-Derived Neurotrophic Factor: BDNF)とは?
BDNFは、神経細胞の成長や生存、そしてシナプスの強化(これにより学習や記憶が向上します)を助けます。BDNFは特に海馬や前頭前皮質など、記憶や思考に関わる脳の部分で多く見られます。脳卒中患者さんは、健常者と比べると血中のBDNF濃度が低下していることがわかっています。近年、BDNFを増やすことで病気の治療や予防に役立てようとする動きがあります。
高強度トレーニングのデメリット
一方で、高強度トレーニングには以下のデメリットがあることが考えられています。
- 関節痛や腰痛の出現
運動強度が高い分、筋肉をたくさん使うため、痛みが出やすいという報告があります。
一方で、こういった有害事象の報告は高強度トレーニングが他のリハビリ方法よりも特別に高いわけではないことも報告されています(Luo L, 2019; Mah SM, 2020)。
患者様の状態に合わせて、運動強度を調整しながら進めるのが重要と言えます。
BRAINで高強度トレーニングを行うときは、低強度から開始して徐々に強度を上げていくことをオススメしています。
担当セラピストさんと一緒に、ご自身に合った強度設定を行い、取り組んでみてください。
有酸素運動と筋力増強訓練

有酸素運動と筋力増強訓練とは?
有酸素運動は歩行練習やジョギング、サイクリングなどのことを指します。
筋力増強訓練は、いわゆる筋力トレーニング(以下、筋トレ)のことです。
脳卒中後の歩行リハビリにおいて、有酸素運動と筋トレを組み合わせることが有効であると報告されています。
有酸素運動と筋力増強訓練の効果・メリット
以下の効果が報告されています(Pogrebnoy D, 2020; Lee J, 2020)。
歩行持久力を向上させる
また、有酸素運動については脳卒中再発予防に役立つことが報告されています。
再発予防について詳しく知りたい方はこちらの記事をご覧ください。
有酸素運動と筋力増強訓練のデメリット
有酸素運動と筋力増強訓練に目立ったデメリットはありません。
怪我や転倒などの有害事象については、特別に多いわけではないことが報告されています(Pogrebnoy D, 2020; Lee J, 2020)。
細かい注意点ですが、運動強度を間違えると『運動したのに効果が得られなかった』ということが起こりますので、専門家の指導のもと行うのが望ましいと言えるでしょう。
ロボットアシストトレーニング
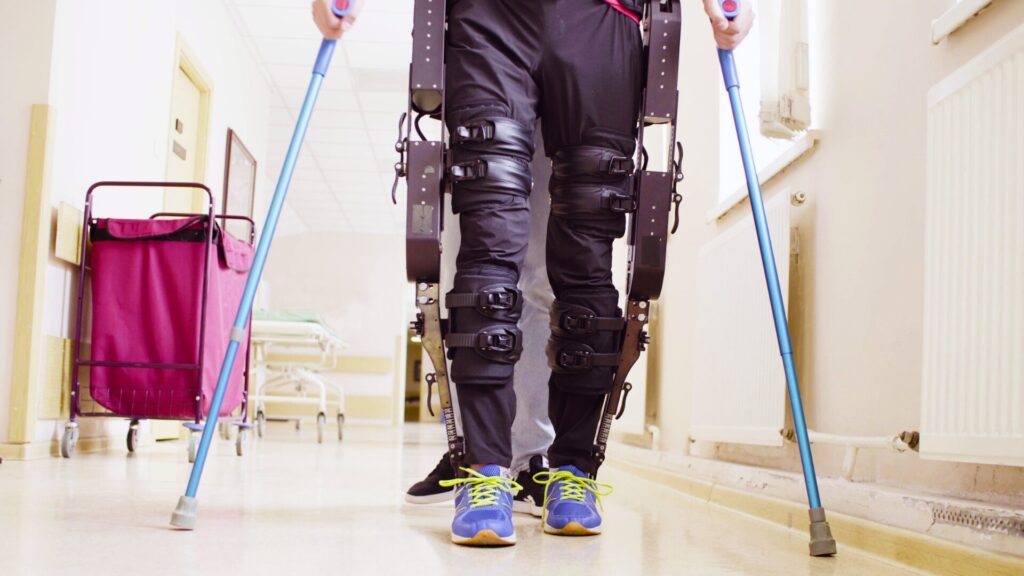
ロボットアシストトレーニングとは?
ロボットを使って歩く練習をするものです。
ロボットは以下の2つに大別されます。
- エンドエフェクター型…通常の歩行練習をベースとし、それをサポートする小型のロボット
- エクソスケルトン型…外骨格型とも呼ばれ、患者さんに装着して歩行練習を行う大型のロボット
現状、こういったロボットの種類にかかわらず、ロボットを使って歩行練習を行うものをロボットアシストトレーニングといいます。
ロボットアシストトレーニングの効果・メリット
ロボットアシストトレーニングは、以下の効果があることが報告されています(Mehrholz J, 2020; Cho JE, 2018; Maranesi E, 2020; Nedergård H, 2021; Moucheboeuf G, 2020; Calafiore D, 2022; Mehrholz J, 2018)。
- 歩行速度を向上させる
- 歩行持久力を向上させる
- 歩きかたをきれいにする
- 歩行自立度を向上させる
このように、ロボットアシストトレーニングは歩行における4つの問題すべてに対応できることが知られています。
ロボットアシストトレーニングのデメリット
ロボットは世界各国で開発・研究されており、たくさんの種類があります。
国内でも『ロボットを使った歩行リハビリ』を売りにしている施設がありますが、ロボットなら何でも有効というわけではありません。
例えば、Mehrholz Jら(2018)は、エンドエフェクター型は歩行持久力を向上させる効果があるものの、エクソスケルトン型には歩行持久力を向上させる効果を期待できないことを報告しています。
このように、全体で見れば有効であるものの、部分で見れば有効とは言えない、というケースも散見されます。
ロボットアシストトレーニングを行う際は、『ロボットアシストトレーニング全体のエビデンス』だけでなく、『ご自身が使うロボットのエビデンス』を担当セラピストさんに確認するようにしてください。
電気刺激

電気刺激とは?
脚(足)に電気刺激を与えて筋肉を収縮させることです。
一般的に、脳卒中を発症すると運動障害(運動麻痺)が生じ、足においては特に足関節背屈(つま先を持ち上げる運動)が行いにくくなります。
これに対し、短下肢装具が処方・作製されることが一般的です。
近年の研究では、短下肢装具の代わりに電気刺激を利用することによって、足関節背屈の運動をサポートすることの有効性が報告されてきています。
電気刺激の効果・メリット
脳卒中後の歩行における電気刺激の効果は以下の通りです(Dunning K, 2015; Lin S, 2018; Prenton S, 2018; Bethoux F, 2014; Bethoux F, 2015)。
- 歩行速度を向上させる
- 麻痺側下肢の運動機能を向上させる
上述の通り、歩行中に電気刺激を使うことによって足関節背屈をサポートし、歩きやすくしてくれます。
短下肢装具と同等の効果を持つことが知られており、近年では短下肢装具を外して電気刺激装置を装着し、外出される方もいらっしゃいます。
短下肢装具を外して歩けるようになる条件について詳しく知りたい方はこちらの記事をご覧ください。
なお、電気刺激には
- 歩行練習に電気刺激を併用させる方法
- 歩行練習に併用しないで電気刺激を与える方法
の2つがあります。
上記でお伝えしたのは前者による効果・メリットであり、後者による効果・メリットはまた異なります。
電気刺激について詳しく知りたい方はこちらの記事をご覧ください。
電気刺激のデメリット
デメリットは以下の通りです。
- 事故のリスクがある
- 電気のセッティングに時間がかかる
電気刺激には『禁忌』があり、禁忌に該当する状態の方は電気刺激を受けることができません。
禁忌に該当する状態で電気刺激を行ってしまうと、お怪我などの事故が生じる危険性があります。
電気刺激の禁忌について詳しく知りたい方はこちらをご覧ください。
事故を防ぐため、電気刺激の使用は専門家のもとで行うことをお勧めします。
頻回な歩行練習

ガイドラインで推奨されているリハビリ方法(トレッドミルや電気刺激など)でも、少ししか行わないのであれば効果を期待することはできません。
Mehrholz Jら(2017)は、トレッドミルで歩行速度を上げる場合は週3回以上、歩行持久力を向上させる場合は週5回以上のリハビリを行う必要があることを報告しています。
つまり、歩行をよくするためには週3〜5回以上のリハビリを行う必要があるということです。
有効とは言えない歩行リハビリ3選

一般的に行われているものの、有効性が否定されているリハビリ方法を紹介します。
ボバース・コンセプト
ボバース・コンセプトに基づくリハビリは、有効性について懐疑的な意見・データが多いです。
Scrivener Kら(2020)は世界中のエビデンスを集めて解析した結果、ボバースは他のリハビリと比べたときに有効とは言えないと結論付けています。
また、同研究でボバースは筋トレと同等の効果であると報告されています。
上述の通り、筋トレ単体では歩行能力を改善させる効果はあると言えません。
したがって、歩行をよくするためにボバースを行うのは、改善の視点から見れば望ましくないと言えます。
実際、Lennonら(2006)は、ボバースに精通した理学療法士に歩行リハビリを行わせても、脳卒中患者さんの歩きかたは改善したと言えない結果になったことを報告しています。
本研究では、ボバースの基礎講習会、上級講習会を修了した経験年数14年以上の理学療法士が、ボバース概念に基づく理学療法を行っています。
平均介入期間は17.4週(8〜35週間)で、週2〜3回または毎日リハビリが行われました。
ボバース概念に基づく理学療法の前後でいくつかの評価項目に変化が認められましたが、主要な評価である歩行速度や歩きかた(歩容)については変化(改善)したとは言えないという結果になっています。
また、日本国内からの報告もあります。
2009年にボバース記念病院の医師が報告した研究では、BWSTTによる歩行練習に加え、セラピストの促通技法(facilitation technique)を行い、その効果を検証しました。
促通技法は、BWSTTで歩く練習をしているときに、セラピストが患者さんの骨盤や股関節を操作し、股関節と骨盤領域への継続的な感覚運動刺激を提供するものです。
ボバース・セラピストが行う促通技法が歩行に有効なのであれば、促通技法を行うことで、歩行能力がより大きく改善するはずです。
しかし、結果として、促通技法を行なっても大きく改善するとは言えないと報告されました。
『ボバースの病院で働いているセラピストが促通技法を行った上でこの結果である』ということが、『ボバースの病院から報告されている』、ということは重要な意味を持つと言えるでしょう。
ボバース・コンセプトの効果について詳しく知りたい方はこちらをご覧ください。
これらのことから、歩行リハビリとしてボバースを行うのは望ましくないと言えます。
筋力トレーニング
筋力トレーニングは、有酸素運動と組み合わせると歩行に有効ですが、筋トレだけでは歩行に有効とは言えません。
Wist Sら(2016)は脳卒中患者さんへの筋力トレーニングの効果を検証した結果、『筋トレは筋力を向上させるものの、バランスや歩行能力を改善させるとは言えない』と結論づけています。
筋力はバランスや歩行を構成する大事な要素のひとつですが、筋力を上げるだけではダメだということです。
筋トレと併用して、バランス練習や歩行練習(有酸素運動)を行うことが求められます。
短時間・低頻度の歩行練習
歩行リハビリの成果は、リハビリの『方法』と『時間・頻度』によって決まります。
方法については、
- ガイドラインで推奨されているリハビリ方法(トレッドミルや電気刺激など)を選択する
- 筋トレ単体やボバースを行うことを避ける
を守っていれば問題はありません。
一方、時間・頻度については注意が必要です。
ガイドラインで推奨されているリハビリ方法(トレッドミルや電気刺激など)を選択しても、
- 10分しか歩かない
- 週1回しかリハビリをしない
では、効果を期待することはできません。
歩行の改善を報告した研究のほとんどで、1回あたり30分以上の歩行練習が行われています。
つまり、歩行リハビリは1回あたり30分以上は行うべきであると言えます。
上述の通り、Mehrholz Jら(2017)は、トレッドミルで歩行速度を上げる場合は週3回以上、歩行持久力を向上させる場合は週5回以上のリハビリを行う必要があることを報告しています。
まとめると、
- ガイドラインで推奨されているリハビリ方法(トレッドミルや電気刺激など)を選択する
- 1回あたり30分以上は歩く
- 週3〜5回以上は歩行リハビリを行う
ことが歩行を改善させる上で必要であると言えます。
まとめ
本記事のまとめです。
- 脳卒中後の歩行における問題として『歩行速度』『歩行距離(歩行持久力)』『歩きかた』『歩行自立度』の4つの問題がある
- これらの問題を解決するためには有効性が実証されたリハビリ方法を、適切な条件で行うことが大事
専門家の指導のもと、歩行の問題点を分析し、適切なリハビリを受けられるようにしましょう。
リハビリの無料体験を実施中!
といった方から選ばれています!

BRAINアカデミー
エビデンスに基づく脳卒中リハビリテーションを体系的・網羅的に学ぶ、6ヶ月間のオンライン学習プログラムです。①動画教材 ②課題 ③フィードバックを通じて、EBMを身に付けましょう!
詳細はこちら

文献検索CAMP
PubMedを使った文献検索を2日でマスターするセラピスト向けオンライン学習プログラムです。AIを活用し、経験1年目の方でも文献検索を行えるレベルまでスキルアップできます。
詳細はこちら
参考文献
Lee KB, Kim JS, Hong BY, Sul B, Song S, Sung WJ, Hwang BY, Lim SH. Brain lesions affecting gait recovery in stroke patients. Brain Behav. 2017 Oct 25;7(11):e00868.
Gomez Bernal A, Becerro-de-Bengoa-Vallejo R, Losa-Iglesias ME. Reliability of the OptoGait portable photoelectric cell system for the quantification of spatial-temporal parameters of gait in young adults. Gait Posture. 2016;50:196-200.
Chui KK, Lusardi MM. Spatial and temporal parameters of self-selected and fast walking speeds in healthy community-living adults aged 72-98 years. J Geriatr Phys Ther. 2010;33(4):173-83.
Sheffler LR, Chae J. Hemiparetic Gait. Phys Med Rehabil Clin N Am. 2015 Nov;26(4):611-23.
Balaban B, Tok F. Gait disturbances in patients with stroke. PM R. 2014 Jul;6(7):635-42.
Roelker SA, Bowden MG, Kautz SA, Neptune RR. Paretic propulsion as a measure of walking performance and functional motor recovery post-stroke: A review. Gait Posture. 2019 Feb;68:6-14.
An S, Lee Y, Shin H, Lee G. Gait velocity and walking distance to predict community walking after stroke. Nurs Health Sci. 2015 Dec;17(4):533-8.
田代英之・他:慢性期脳卒中者の地域における移動能力と歩行機能および身体活動の関係. 理学療法学. 2014. 41(3) 131-137
Kubo H, Nozoe M, Kanai M, Furuichi A, Onishi A, Kajimoto K, Mase K, Shimada S. Reference value of 6-minute walk distance in patients with sub-acute stroke. Top Stroke Rehabil. 2020 Jul;27(5):337-343.
Kramer S, Johnson L, Bernhardt J, Cumming T. Energy Expenditure and Cost During Walking After Stroke: A Systematic Review. Arch Phys Med Rehabil. 2016 Apr;97(4):619-632.e1.
Mehrholz J, Thomas S, Elsner B. Treadmill training and body weight support for walking after stroke. Cochrane Database Syst Rev. 2017 Aug 17;8
Bishnoi A, Lee R, Hu Y, Mahoney JR, Hernandez ME. Effect of Treadmill Training Interventions on Spatiotemporal Gait Parameters in Older Adults with Neurological Disorders: Systematic Review and Meta-Analysis of Randomized Controlled Trials. Int J Environ Res Public Health. 2022 Feb 28;19(5):2824.
Srivastava, Abhishek, et al. “Bodyweight-supported treadmill training for retraining gait among chronic stroke survivors: A randomized controlled study.” Annals of physical and rehabilitation medicine 59.4 (2016): 235-241.
Nascimento LR, Boening A, Galli A, Polese JC, Ada L. Treadmill walking improves walking speed and distance in ambulatory people after stroke and is not inferior to overground walking: a systematic review. J Physiother. 2021 Apr;67(2):95-104.
Luo L, Zhu S, Shi L, Wang P, Li M, Yuan S. High Intensity Exercise for Walking Competency in Individuals with Stroke: A Systematic Review and Meta Analysis. J Stroke Cerebrovasc Dis. 2019 Dec;28(12):104414.
Mah SM, Goodwill AM, Seow HC, Teo WP. Evidence of High-Intensity Exercise on Lower Limb Functional Outcomes and Safety in Acute and Subacute Stroke Population: A Systematic Review. Int J Environ Res Public Health. 2022 Dec 22;20(1):153.
Boyne P, Meyrose C, Westover J, Whitesel D, Hatter K, Reisman DS, Cunningham D, Carl D, Jansen C, Khoury JC, Gerson M, Kissela B, Dunning K. Exercise intensity affects acute neurotrophic and neurophysiological responses poststroke. J Appl Physiol (1985). 2019 Feb 1;126(2):431-443.
Li X, Charalambous CC, Reisman DS, Morton SM. A short bout of high-intensity exercise alters ipsilesional motor cortical excitability post-stroke. Top Stroke Rehabil. 2019 Sep;26(6):405-411.
Pogrebnoy D, Dennett A. Exercise Programs Delivered According to Guidelines Improve Mobility in People With Stroke: A Systematic Review and Meta-analysis. Arch Phys Med Rehabil. 2020 Jan;101(1):154-165.
Lee J, Stone AJ. Combined Aerobic and Resistance Training for Cardiorespiratory Fitness, Muscle Strength, and Walking Capacity after Stroke: A Systematic Review and Meta-Analysis. J Stroke Cerebrovasc Dis. 2020 Jan;29(1):104498.
Mehrholz J, Thomas S, Kugler J, Pohl M, Elsner B. Electromechanical-assisted training for walking after stroke. Cochrane Database Syst Rev. 2020 Oct 22;10(10):CD006185.
Cho JE, Yoo JS, Kim KE, Cho ST, Jang WS, Cho KH, Lee WH. Systematic Review of Appropriate Robotic Intervention for Gait Function in Subacute Stroke Patients. Biomed Res Int. 2018 Feb 6;2018:4085298.
Maranesi E, Riccardi GR, Di Donna V, Di Rosa M, Fabbietti P, Luzi R, Pranno L, Lattanzio F, Bevilacqua R. Effectiveness of Intervention Based on Endeffector Gait Trainer in Older Patients With Stroke: A Systematic Review. J Am Med Dir Assoc. 2020 Aug;21(8):1036-1044.
Nedergård H, Arumugam A, Sandlund M, Bråndal A, Häger CK. Effect of roboticassisted gait training on objective biomechanical measures of gait in persons post-stroke: a systematic review and meta-analysis. J Neuroeng Rehabil. 2021 Apr 16;18(1):64.
Moucheboeuf G, Griffier R, Gasq D, Glize B, Bouyer L, Dehail P, Cassoudesalle H. Effects of robotic gait training after stroke: A meta-analysis. Ann Phys Rehabil Med. 2020 Nov;63(6):518-534.
Calafiore D, Negrini F, Tottoli N, Ferraro F, Ozyemisci-Taskiran O, de Sire A. Efficacy of robotic exoskeleton for gait rehabilitation in patients with subacute stroke : a systematic review. Eur J Phys Rehabil Med. 2022 Feb;58(1):1-8.
Mehrholz J, Pohl M, Kugler J, Elsner B. The Improvement of Walking Ability Following Stroke. Dtsch Arztebl Int. 2018 Sep 28;115(39):639-645.
Dunning K, O’Dell MW, Kluding P, McBride K. Peroneal Stimulation for Foot Drop After Stroke: A Systematic Review. Am J Phys Med Rehabil. 2015 Aug;94(8):649-64.
Lin S, Sun Q, Wang H, Xie G. Influence of transcutaneous electrical nerve stimulation on spasticity, balance, and walking speed in stroke patients: A systematic review and meta-analysis. J Rehabil Med. 2018 Jan 10;50(1):3-7.
Prenton S, Hollands KL, Kenney LPJ, Onmanee P. Functional electrical stimulation and ankle foot orthoses provide equivalent therapeutic effects on foot drop: A meta-analysis providing direction for future research. J Rehabil Med. 2018 Feb 13;50(2):129-139.
Bethoux F, Rogers HL, Nolan KJ, Abrams GM, Annaswamy TM, Brandstater M, Browne B, Burnfield JM, Feng W, Freed MJ, Geis C, Greenberg J, Gudesblatt M, Ikramuddin F, Jayaraman A, Kautz SA, Lutsep HL, Madhavan S, Meilahn J, Pease WS, Rao N, Seetharama S, Sethi P, Turk MA, Wallis RA, Kufta C. The effects of peroneal nerve functional electrical stimulation versus ankle-foot orthosis in patients with chronic stroke: a randomized controlled trial. Neurorehabil Neural Repair. 2014 Sep;28(7):688-97.
Bethoux F, Rogers HL, Nolan KJ, Abrams GM, Annaswamy T, Brandstater M, Browne B, Burnfield JM, Feng W, Freed MJ, Geis C, Greenberg J, Gudesblatt M, Ikramuddin F, Jayaraman A, Kautz SA, Lutsep HL, Madhavan S, Meilahn J, Pease WS, Rao N, Seetharama S, Sethi P, Turk MA, Wallis RA, Kufta C. Long-Term Follow-up to a Randomized Controlled Trial Comparing Peroneal Nerve Functional Electrical Stimulation to an Ankle Foot Orthosis for Patients With Chronic Stroke. Neurorehabil Neural Repair. 2015 Nov-Dec;29(10):911-22.
Wist S, Clivaz J, Sattelmayer M. Muscle strengthening for hemiparesis after stroke: A meta-analysis. Ann Phys Rehabil Med. 2016 Apr;59(2):114-24.
Scrivener K, Dorsch S, McCluskey A, Schurr K, Graham PL, Cao Z, Shepherd R, Tyson S. Bobath therapy is inferior to task-specific training and not superior to other interventions in improving lower limb activities after stroke: a systematic review. J Physiother. 2020 Oct;66(4):225-235.
Lennon S, Ashburn A, Baxter D. Gait outcome following outpatient physiotherapy based on the Bobath concept in people post stroke. Disabil Rehabil. 2006 Jul 15-30;28(13-14):873-81.
Yagura H, Hatakenaka M, Miyai I. Does therapeutic facilitation add to locomotor outcome of body weight–supported treadmill training in nonambulatory patients with stroke? A randomized controlled trial. Arch Phys Med Rehabil. 2006 Apr;87(4):529-35.











